fenilalanina è un aminoacido proteinogenico essenziale con un anello aromatico a sei membri che funge da elemento costitutivo di molte proteine e peptidi.
Inoltre, la fenilalanina svolge un ruolo importante nel metabolismo dell'azoto e può essere convertita nel fegato nell'amminoacido proteinogenico della tirosina. La fenilalanina e la tirosina svolgono un ruolo importante nella sintesi di insulina, melanina, tiroxina e neurotrasmettitori dopamina, serotonina e tiramina.
Cos'è la fenilalanina?
La fenilalanina è un alfa-amminoacido essenziale che, a differenza della maggior parte degli amminoacidi proteinogenici, non è solo bioattivo nella forma L, ma in misura limitata anche come enantiomero nella forma R.
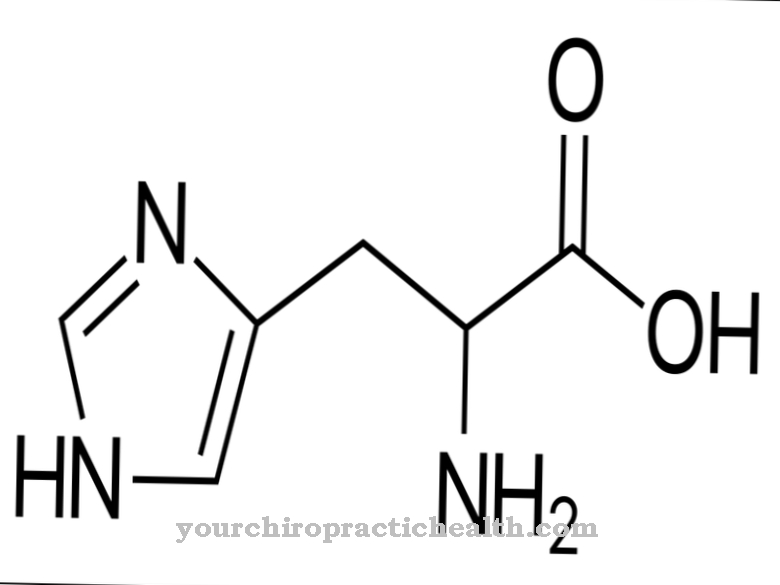
La R-fenilalanina è biochimicamente in gran parte inattiva e si verifica esclusivamente nella produzione artificiale dell'amminoacido, ma è in discussione il ruolo della D-fenilalanina nel controllo di alcuni neurotrasmettitori all'interno del complesso del dolore. Come caratteristica strutturale caratteristica, la fenilalanina ha un semplice anello aromatico a sei membri (anello benzenico) con una catena di idrocarburi attaccata. La formula chimica di struttura è C6H5-CH2-CH (NH2) -COOH, con il gruppo C6H5 che indica l'anello benzenico. L'amminoacido è anfifilico, il che significa che è sia grasso che solubile in acqua.
La formula chimica mostra anche che la fenilalanina è composta esclusivamente da carbonio, idrogeno, azoto e ossigeno, sostanze onnipresenti. Metalli rari, minerali o oligoelementi non fanno parte dell'amminoacido. Tuttavia, il metabolismo umano non può sintetizzare la fenilalanina in misura sufficiente dalla tirosina, ma dipende dall'assunzione dal cibo. La fenilalanina è presente in quantità sufficiente in molti alimenti sia animali che vegetali, tanto che con una normale dieta mista - assumendo un normale assorbimento nel tratto digerente - non c'è carenza di amminoacido da temere.
Funzione, effetto e compiti
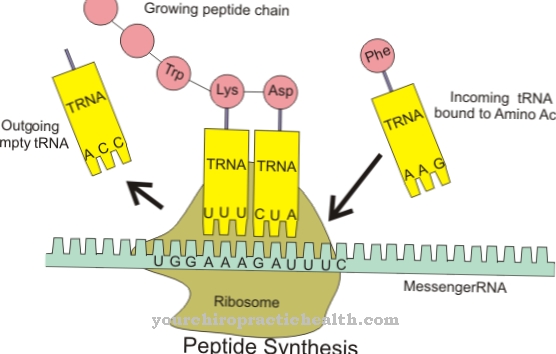
La funzione e il compito più importanti della fenilalanina è partecipare alla struttura di molte proteine e peptidi. Inoltre è coinvolto nella sintesi di alcuni ormoni che svolgono un ruolo centrale nel controllo dei processi metabolici.
Esistono ormoni come l'adrenalina, la noradrenalina, la L-dopa, la PEA e la melanina. Inoltre, la L-fenilalanina funge da sostanza di base da cui z. B. la sostanza messaggera dopamina, serotonina, tiramina e altri possono essere sintetizzati. La L-fenilalanina serve anche come materiale di partenza per l'amminoacido essenziale tirosina. A tale scopo, la fenilalanina viene convertita in tirosina nel fegato in due fasi mediante idrossilazione e scissione di una molecola d'acqua. La fenilalanina idrossilasi è l'enzima che catalizza la conversione in tirosina.
Un apporto alternativo dell'amminoacido anche essenziale tirosina può, come con la fenilalanina, avvenire attraverso l'assunzione di cibo. A differenza di tutti gli altri amminoacidi, che mostrano solo effetti bioattivi nella loro forma L, l'enantiomero D della fenilalanina sembra avere almeno un'influenza sulla percezione del dolore. È stato riscontrato che una miscela di L- e D-fenilalanina (miscela racemica) ha un effetto analgesico. È probabile che la miscela DL blocchi la degradazione delle encefaline - gli oppioidi del corpo - in modo che l'effetto analgesico sia prolungato e intensificato.
Istruzione, occorrenza, proprietà e valori ottimali
L'amminoacido essenziale fenilalanina viene assorbito attraverso il cibo. Non è libero, ma di solito come parte di una proteina o di un polipeptide in forma legata chimicamente. Per rendere disponibile l'aminoacido per il metabolismo, la proteina corrispondente deve essere prima scomposta nel corso della digestione e quindi estratta dai "frammenti" utilizzando ulteriori enzimi nell'ulteriore metabolismo.
La L-fenilalanina è sintetizzata attraverso la cosiddetta via dell'acido shikimico. È una complessa reazione a catena biocatalitica che hanno piante e batteri autotrofi. La particolarità degli organismi autotrofi è la loro capacità di formare materia organica da materiale esclusivamente inorganico. La L-fenilalanina libera ha un sapore amaro, mentre il suo enantiomero D, prodotto esclusivamente nella produzione industriale, ha un sapore dolce. L'amminoacido è z. B. offerto come integratore alimentare e fa anche parte del dolcificante artificiale aspartame. La L-fenilalanina biodisponibile si trova in forma legata in molti alimenti.
Il loro contenuto è particolarmente elevato nei piselli secchi e nei semi di soia, nelle noci e nei semi di zucca, nonché in vari tipi di pesce e carne. Il fabbisogno di fenilalanina dipende fortemente dalla fornitura di tirosina. Se non c'è tirosina nella dieta, il corpo ha bisogno di 38-52 mg per kg di massa corporea. Con un ricco apporto di tirosina nella dieta, il fabbisogno giornaliero scende a soli 9 mg per kg di massa corporea. Di norma, gli alimenti contenenti fenilalanina contengono anche una quantità corrispondente di tirosina.
La raccomandazione della FAO / OMS dal 1985 ammonta a un fabbisogno combinato di L-fenilalanina e L-tirosina di 14 mg per kg di massa corporea al giorno. Un adulto con una massa corporea di 80 kg necessita quindi di 1.120 mg di entrambe le sostanze al giorno.
Malattie e disturbi
I sintomi di carenza quando c'è un apporto permanentemente insufficiente di fenilalanina e tirosina nella dieta sono estremamente rari, ma possono avere gravi conseguenze, soprattutto nell'area neuronale.
Oltre a una compromissione della sintesi di molti ormoni e neurotrasmettitori, la carenza può anche essere manifestata da un'interruzione della mielinizzazione delle fibre nervose. L'opposto di una carenza, una concentrazione eccessiva di fenilalanina (fenilchetonuria), può verificarsi a causa di una malattia metabolica genetica. La malattia è ereditaria in maniera autosomica recessiva e porta ad una ridotta produzione dell'enzima fenilalanina idrossilasi, che può convertire la fenilalanina in tirosina.
La ridotta attività enzimatica porta ad un forte aumento dell'amminoacido, a ciò che è noto come fenilchetonuria, perché la conversione in tirosina è anche la via di degradazione della fenilalanina. Allo stesso tempo, manca la tirosina perché il percorso di sintesi è bloccato. Un'altra malattia ereditaria in questo contesto è la sindrome di Hartnup. È un disturbo metabolico che interrompe il trasporto della fenialanina attraverso la membrana cellulare. Questo porta a seri problemi al sistema nervoso centrale, sulla pelle e nel tratto digerente.

.jpg)