A serina è un amminoacido che è uno dei venti amminoacidi naturali e non è essenziale. La forma D della serina agisce come co-agonista nella segnalazione neuronale e può svolgere un ruolo in varie malattie mentali.
Cos'è la serina
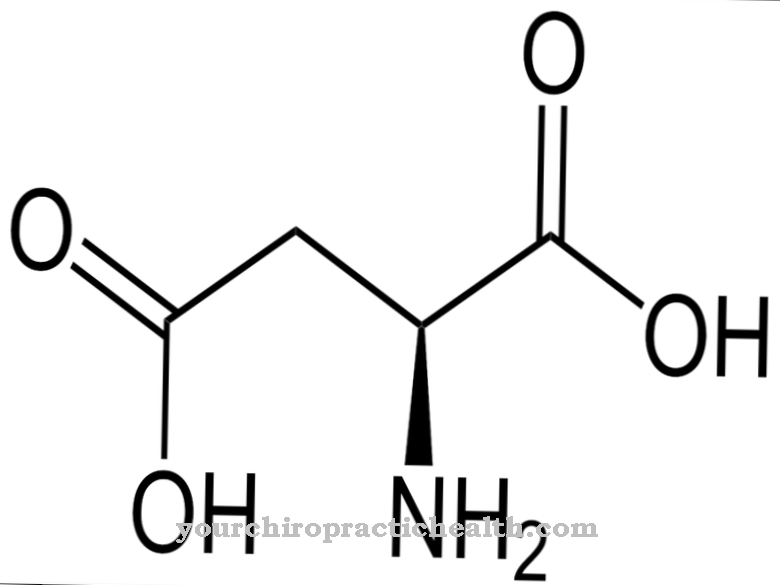
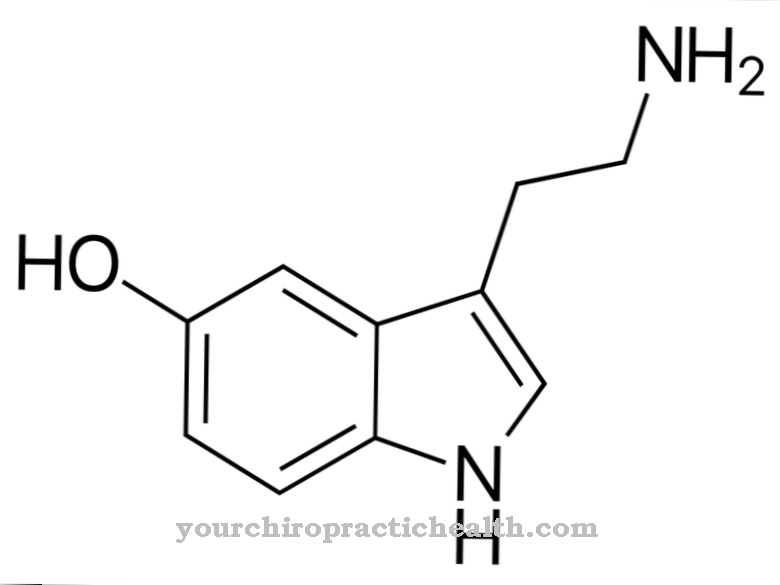
La serina è un amminoacido con la formula strutturale H2C (OH) -CH (NH2) -COOH. Si presenta nella forma L ed è uno degli amminoacidi non essenziali, poiché il corpo umano può produrlo da solo. La serina deve il suo nome alla parola latina "sericum", che significa "seta".
La seta può servire come materia prima per la serina elaborando tecnicamente la sericina della colla di seta. Come tutti gli amminoacidi, la serina ha una struttura caratteristica. Il gruppo carbossilico è costituito dalla sequenza atomica carbonio, ossigeno, ossigeno, idrogeno (COOH); il gruppo carbossilico reagisce in modo acido quando uno ione H + viene scisso. Il secondo gruppo di atomi è il gruppo amminico. È composto da un atomo di azoto e due atomi di idrogeno (NH2).
A differenza del gruppo carbossilico, il gruppo amminico ha una reazione di base in quanto attacca un protone alla coppia solitaria di elettroni sull'azoto. Sia il gruppo carbossile che il gruppo amminico sono gli stessi per tutti gli amminoacidi. Il terzo gruppo di atomi è la catena laterale, a cui gli amminoacidi devono le loro diverse proprietà.
Funzione, effetto e compiti
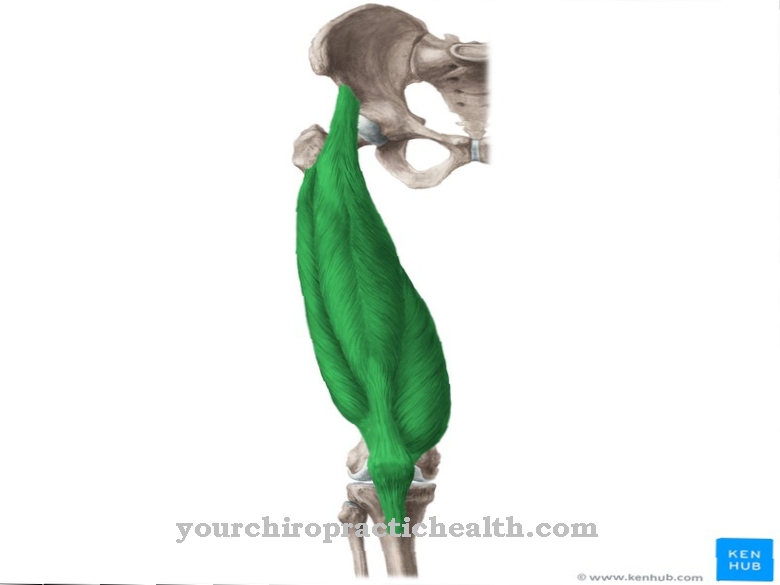
La serina ha due importanti funzioni per il corpo umano. In quanto amminoacido, la serina è un elemento costitutivo delle proteine, che sono macromolecole e formano enzimi e ormoni, nonché sostanze di base come actina e miosina che compongono i muscoli.
Anche gli anticorpi del sistema immunitario e l'emoglobina, il pigmento rosso del sangue, sono proteine. Oltre alla serina, ci sono diciannove altri amminoacidi che si trovano nelle proteine naturali. La disposizione specifica degli amminoacidi crea lunghe catene proteiche. A causa delle loro proprietà fisiche, queste catene si piegano e formano una struttura spaziale tridimensionale. Il codice genetico determina l'ordine degli amminoacidi all'interno di tale catena.
Nella maggior parte delle cellule umane, la serina è nella sua forma L. Al contrario, la D-serina viene prodotta nelle cellule del sistema nervoso: i neuroni e le cellule gliali. In questa variante, la serina agisce come un co-agonista: si lega ai recettori delle cellule nervose e quindi innesca un segnale nel neurone che trasmette come impulso elettrico al suo assone e in avanti alla cellula nervosa successiva. In questo modo, il trasferimento delle informazioni avviene all'interno del sistema nervoso.
Tuttavia, una sostanza messaggera non può legarsi a tutti i recettori a piacimento: secondo il principio di blocco e chiave, i neurotrasmettitori e i recettori devono avere proprietà che corrispondono tra loro. La D-serina si presenta, tra le altre cose, come co-agonista dei recettori NMDA. Sebbene la serina non sia la principale sostanza messaggera lì, ha un effetto rinforzante sulla trasmissione del segnale.
Istruzione, occorrenza, proprietà e valori ottimali
La serina è essenziale per il funzionamento del corpo. Le cellule umane formano la serina ossidando e amminando il 3-fosfoglicerato, cioè aggiungendo un gruppo amminico. La serina è uno degli amminoacidi neutri: il suo gruppo amminico ha un valore di pH equilibrato e quindi non è né acido né basico. Inoltre, la serina è un amminoacido polare.
Poiché è uno degli elementi costitutivi di tutte le proteine umane, è molto comune. La serie L è la variante naturale della serina e si presenta principalmente a un pH neutro di circa sette. Questo valore di pH prevale all'interno delle cellule del corpo umano, in cui viene elaborata la serina. La L-serina è uno zwitterion. Uno zwitterione si crea quando il gruppo carbossilico e il gruppo amminico reagiscono tra loro: il protone del gruppo carbossilico migra al gruppo amminico e lì si attacca alla coppia solitaria di elettroni.
Di conseguenza, lo zwitterion ha una carica sia positiva che negativa ed è completamente scarico. Il corpo spesso scompone la serina in glicina, che è anche un amminoacido che, come la serina, è neutro ma non polare. La serina può anche produrre piruvato, noto anche come acido acetilformico o acido piruvico. È un acido cheto carbossilico.
Malattie e disturbi
Nella sua forma L, la serina si trova nei neuroni e nelle cellule gliali e probabilmente svolge un ruolo in varie malattie mentali. La L-serina si lega come co-agonista ai recettori N-metil-D-aspartato, o recettori NMDA in breve. Rafforza l'effetto del neurotrasmettitore glutammato, che si lega ai recettori NMDA e quindi attiva le cellule nervose.
I processi di apprendimento e memoria dipendono dai recettori NMDA; indica il rimodellamento delle connessioni sinaptiche e quindi modifica la struttura del sistema nervoso. Questa plasticità si esprime come apprendimento a livello macro. La scienza considera questa connessione rilevante per la malattia mentale. Le malattie mentali portano a numerose menomazioni funzionali, che spesso includono anche problemi di memoria. Anche i processi di apprendimento difettosi possono contribuire allo sviluppo della malattia mentale. Un esempio di questo è la depressione. La depressione porta a scarse prestazioni cognitive, soprattutto quando è molto grave. Tuttavia, l'apprendimento e le prestazioni della memoria migliorano di nuovo quando la depressione si attenua.
Una teoria attuale presume che l'attivazione frequente di alcune vie nervose aumenti la probabilità che queste vie vengano attivate più rapidamente con stimoli futuri: la soglia dello stimolo si abbassa. Questa considerazione si basa su uno sblocco dei recettori, che potrebbe spiegare il processo. Nel caso di malattie mentali come la depressione o la schizofrenia, potrebbe esserci un'interruzione in questo processo, che può spiegare almeno una parte dei rispettivi sintomi. In questo contesto, gli studi iniziali confermano l'effetto della D-serina come antidepressivo.




.jpg)

.jpg)
.jpg)